����[����]
����26.(13��)
�����������(Fe)ȥ��ˮ���е�������(NO3��)�ѳ�Ϊ�������о����ȵ�֮һ��
����(1)Fe��ԭˮ����NO3���ķ�Ӧԭ������ͼ��ʾ��
����
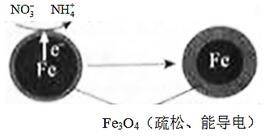
��������������������________��
�����������ĵ缫��Ӧʽ��_________��
����(2)����������Ͷ��ˮ���У���24Сʱ�ⶨNO3����ȥ���ʺ�pH��������£�
����

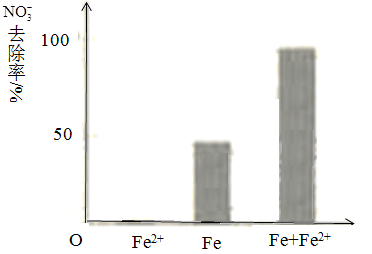
����(3)ʵ�鷢�֣��ڳ�ʼpH=4.5��ˮ����Ͷ���������۵�ͬʱ������һ������Fe2+�����������NO3����ȥ���ʡ���Fe2+������������ּ��裺pH=4.5ʱ��NO3����ȥ���ʵ͡���ԭ����________��
������. Fe2+ֱ�ӻ�ԭNO3��;
������. Fe2+�ƻ�FeO(OH)�����㡣
���������Ա�ʵ�飬�������ͼ��ʾ���ɵõ��Ľ�����_______��
������ͬλ��ʾ�ٷ�֤ʵFe2+����FeO(OH)��Ӧ����Fe3O4����ϸ÷�Ӧ�����ӷ���ʽ�����ͼ���Fe2+���NO3��ȥ���ʵ�ԭ��______��
����
����pH =4.5(����������ͬ)
����(4)����������(2)��ͬ����1Сʱ�ⶨNO3����ȥ���ʺ�pH��������£�
������(2)�����ݶԱȣ�����(2)�г�ʼpH��ͬʱ��NO3��ȥ���ʺ���������������̬��ͬ��ԭ��__________��
����[����]
�����������Ϊһ������ԭ���⣬��ʵҲ��һЩ�Ƚϼ���Ŀ����������1����д������Ӧ�����ʣ�����д������Ӧ���������ɸ����ӣ�İ������ʽ��д���������и߿��������������յļ��ܡ���Ȼ���Ǹ��缫��Ӧ���缫��ӦҲ��İ���ķ���ʽ����İ������ʽ��д��˼·û�����𡣾���24Сʱ֮�����4.5��ʱ�����ȥ���ʵͣ�ԭ����ʲô���ⲿ�ֿ��ܾͻ�����鷳һ�㣬������뵽���ǡ���Ҳ�ǻ�ѧ�����治̫�ý����С���⣬�ܶ�ʱ���뵽�ľ��ǣ��벻���ͺ����Ρ���������������֪�������������Ӱ�����Ӧ�����ѧ�����ʱ��϶���ʦ��ǿ��������������������ʿ϶������ڵġ���������߾�������Ե����⡣�Ա�ʵ�飬ǰ���PH2.5������ǿ�������PH4.5����������
����[����]
����27.(12��)
�����ԷϾ�Ǧ�����еĺ�Ǧ����(Pb��PbO��PbO2��PbSO4��̿�ڵ�)��H2SO4Ϊԭ�ϣ��Ʊ��ߴ�PbO��ʵ��Ǧ���������á��乤���������£�
����

����(1)���̢��У���Fe2+���£�Pb��PbO2��Ӧ����PbSO4�Ļ�ѧ����ʽ��__________��
����(2)���̢��У�Fe2+�����̿ɱ�ʾΪ��
����i��2Fe2++ PbO2+4H++SO42?
����2Fe3++PbSO4+2H2O
����ii: ����
������д��ii�����ӷ���ʽ��________________��
����������ʵ�鷽����֤ʵ���������̡���ʵ�鷽������������
����a.���㻰��FeSO4��Һ�м���KSCN��Һ����Һ������ɫ���ټ�������PbO2����Һ��졣
����b.______________��
����(3)PbO�ܽ���NaOH��Һ�У�����ƽ�⣺PbO(s)+NaOH(aq)
����NaHPbO2(aq)�����ܽ��������ͼ��ʾ��
����
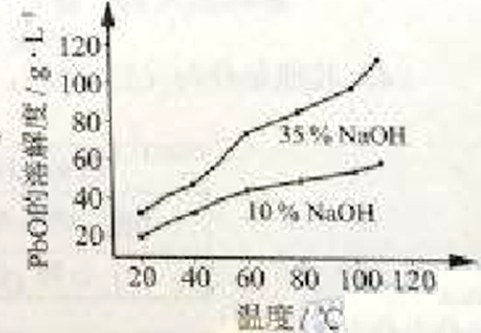
�����ٹ��̢��Ŀ����������Һ1����������ڹ��̢����ظ�ʹ�ã���Ŀ����_____(ѡ�����)��
����[����]
�������ǹ�ҵ�����⣬д����ʽ��Ȼ�����Ӧ������������ʽ��������̣��������֤�����������Ӧ���ַ������������Ӧ��������Ƕ������⣬�����������ӣ���������������죬�������������˵���������ˣ��Ǿ����������ġ����������ܿ����Ļ�����Ӧ��������ˡ�������ʵ���ǽ�������Ҫ֤��һ�����飬�����������һ�����о����ˡ�
��������3�Ǹ�ѡ���⣬�ر����ε���һ��ѡ���ⲻ������ʱ��ѡC���������AB����ʵ����Ҳ���Ǻܸ��ӣ��������̣���˵����2��Ŀǰ��������һ���������������ȥ�������Ǹ���������������ܸ��������Ʒ�Ӧ������Ӧ����һ����Ǧ���������Ƶķ�Ӧ��������ǿ�������������������������
��������3��Ŀ�����ᴿ���ۺ���������Ϣ�����ܽ�ȣ��¶ȸߣ���������Ũ���ܽ⣬�¶ȵͣ��������ƿ������������ᴿ�����ܽ⣬��Ũ�����������¶����ߣ������¶Ȳ���ϡ�ͣ�����Ũ���ֵͣ��ͻ�ȥ�ˡ�
����[����]
����28.(16��)��Na2SO3��Һ�Ͳ�ͬ��������������Һ��Ϊʵ�����̽���ε����ʺ�����Һ�䷴Ӧ�Ķ����ԡ�
����
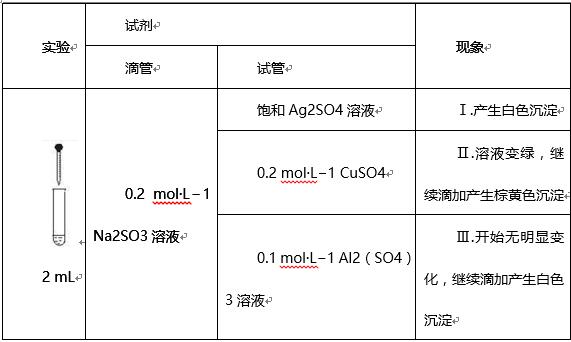
����(2)�����飬�������ػ�ɫ�����в���SO42?������Cu+��Cu2+��SO32?��(1)�����飬������еİ�ɫ������Ag2SO3�������ӷ���ʽ���������____________��
������֪��Cu+
����Cu +Cu2+��Cu2+
����CuI��(��ɫ)+I2��
��������ϡ����֤ʵ�����к���Cu+��ʵ��������_____________��
������ͨ������ʵ��֤ʵ�������к���Cu2+��SO32?��
����
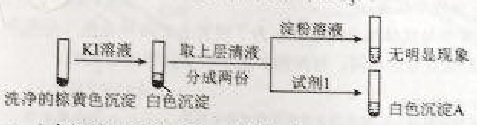
����a.��ɫ����A��BaSO4���Լ�1��____________��
����b.֤ʵ�����к���Cu+��SO32?��������___________��
����(3)��֪��Al2(SO3)3��ˮ��Һ�в����ڡ������飬�����İ�ɫ��������SO42?���ð�ɫ������������ǿ�ᣬ��������ǿ�����ʹ����KMnO4��Һ��ɫ��
�������Ʋ�����к������������________��
�����ڶ��ڳ�������������Ĵ�����ʽ������ּ��裺i.��Al(OH)3������;ii.���������ļ�ʽ���С��Լ���ii����˶Ա�ʵ�飬֤ʵ�˼���ii������
����a.���Ա�ʵ�鷽������������
����

�����������_____________(����ͼ��ʽ����)��
����(4)����ʵ�飬�������ε�������___________������Һ�䷴Ӧ�Ķ�������__________�йء�
����[����]
�����������������һ����ĶԱ�ʵ�飬��Ŀ��ԱȽϸ��ӣ�Ҳ������̽��ʵ��ij���˼·�����ֶԱȣ�������֤������������Ͳ����彲�ˡ��������������Ͼ��������ģ���Ȼ�����˱����������ĸо���ÿһ������һ���ܺõĽ���״�����У�����ͻ���������һ�������ֶȡ�
��������Ƽ���
����2016�߿���![]() | 2016�߿����� | ��ע�ŶԴ� | 2016�߿�����
| 2016�߿����� | ��ע�ŶԴ� | 2016�߿�����
����2016�߿����Ĵ� | 2016�߿���ѧ�� | 2016�߿�Ӣ���
����2016�߿�־Ը� | 2016�߿��ɼ���ѯ | 2016�߿�¼ȡ������

��2021��߿���ѧ��̸�ϰָ�� (2021-5-26 11:20:48)
��2021��߿���ѧ��ϰ���⼼�ɽ�� (2021-5-14 16:30:51)
��2021�߿���ѧ��ϰ���Լ�ע������ (2021-5-12 16:43:19)
��2021��߿���ѧ������ʮ����ԡ� (2021-5-12 16:42:15)
��2021��߿�ǰ���컯ѧ��ϰ���� (2021-5-12 16:40:47)
��������� ��ģ������

2022���Ϻ��߿�������Ŀ�ѹ���
2022����ϸ߿��������ѹ���
2022����ϸ߿�������ѹ���
2022��㶫�߿�����������ѹ���
2022����ϸ߿����������ѹ���
2022��㶫�߿����⼰�𰸻���
2022���㽭�߿����⼰�𰸻���
2022��㶫�߿��������⼰���ѹ���(������)
2022���㽭�߿��������⼰���ѹ���(������)
2022���Ϻ��߿��ɼ���ѯʱ��:7��23��
ɽ��2022�괺���߿��ɼ���ѯ����ѿ�ͨ �����
����2022��߿��ɼ����鷽ʽ
����2022��߿��ɼ���ѯ����ѿ�ͨ �������
ɽ��2022��߿��ɼ���ѯ����ѿ�ͨ �������
2022���㽭�߿��ɼ���ѯ����ѿ�ͨ �������
����2022��߿��ɼ���ѯ����ѿ�ͨ �������
����2022��߿��ɼ���ѯ����ѿ�ͨ �������
����2022��߿��ɼ���ѯ����ѿ�ͨ �������
| ���� | ���� | ��� | �Ϻ� | ���� |
| �ӱ� | ɽ�� | ���� | ���� | ���� |
| �㽭 | ���� | ���� | ���� | ɽ�� |
| ���� | ���� | ���� | �㶫 | ���� |
| ���� | �Ĵ� | ���� | ���� | ���� |
| ���� | ���� | ���� | �ຣ | �½� |
| ������ | ���ɹ� | ���� | ||

